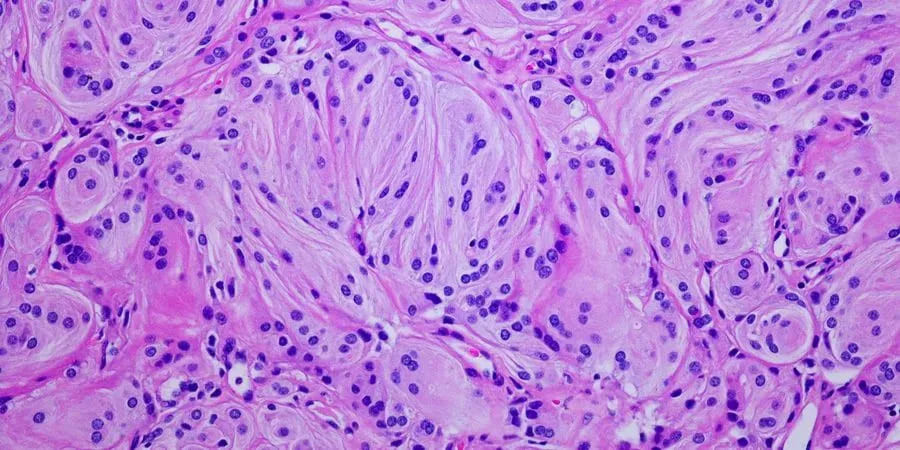
No laboratório e na clínica, a espectroscopia Raman pode ser uma nova abordagem para definir a base molecular da doença e usar esses princípios para revolucionar o diagnóstico
Chandrasekhara Venkata Raman foi uma criança prodígio que obteve seu diploma de pós-graduação aos 19 anos. Ele foi parcialmente encorajado por um caso de identidade equivocada em que o eminente físico britânico Lord Rayleigh dirigiu correspondência pessoal a ele como professor Raman, respondendo ao seu já-problema. trabalho publicado. Naqueles dias, as cores do céu e do mar ainda eram temas quentes em disputa inebriante. Rayleigh já havia identificado a dispersão elástica da luz na atmosfera da Terra que nos faz ver o céu como azul; no entanto, ele também reivindicou o mar azul para um espelho subserviente e reflexivo do céu. Quando Raman atravessou o Mediterrâneo, ele ficou tão impressionado com sua cor que decidiu que não poderia ser, e corrigiu as observações de Rayleigh usando um prisma, espectroscópio,
A carreira de Raman foi fundada em uma série de experimentos em que a luz monocromática adquiria cor e polaridade quando irradiada através de certas amostras líquidas ou cristalinas. Quando os fótons dispersos se movem para estados de energia mais baixos ou mais altos do que os fótons incidentes, os deslocamentos Stokes ou anti-Stokes resultantes podem ser registrados como linhas dentro do espectro Raman. Este espalhamento de luz inelástico é muito mais fraco do que o espalhamento de Rayleigh, e a mudança na frequência corresponde a pequenas mudanças na energia vibracional e rotacional nas ligações químicas dentro das moléculas. O espalhamento Raman pode assim ser quantificado e usado como uma impressão digital molecular, em princípio com equipamentos não muito mais avançados do que o próprio Raman usou.
Embora seja análoga à espectroscopia de infravermelho (IR), a espectroscopia Raman (RS) pode escolher sua fonte monocromática de uma gama muito mais ampla do espectro eletromagnético. Como resultado, ele ficou atrás do IR em utilidade por muitos anos, com fontes de luz disponíveis insatisfatórias que exigiam uma subtração meticulosa de interferência de luz ambiente e fluorescência. O advento dos lasers na década de 1960 e a adição posterior de detectores de carga acoplada melhoraram substancialmente seu rendimento, conveniência e precisão.
Com esses refinamentos técnicos e sua interface em evolução com aprendizado de máquina e algoritmos baseados em informática, o RS está começando a perceber todo o seu poder como ferramenta analítica. Mais significativamente, é uma plataforma que usa uma propriedade fundamental da física para realizar a tarefa química básica comparativamente cotidiana de determinar exatamente o que as coisas são em uma mistura de coisas. Como um procedimento sem reagentes e não destrutivo, é perfeitamente adaptável à medição em laboratório ou em campo , e à biologia em vidro ou em tecido vivo, em que medições repetidas ao longo do tempo têm o poder de informar o tratamento e prognosticar o resultado .
No laboratório e na clínica, a RS pode ser uma nova abordagem para definir a base molecular da doença e usar esses princípios para revolucionar o diagnóstico. O típico aparato Raman de laboratório é exemplificado pelo microscópio confocal Raman Renishaw InVia, que tem sido usado em vários estudos ex vivo de tecido cerebral para discriminar entre matéria branca e cinzenta normal, em comparação com tecido invasivo, tumoral e necrótico, todos com assinaturas espectrais Raman intrínsecas.
Nos cânceres de próstata, pâncreas, mama e ovário, nos quais a detecção precoce é altamente importante e extremamente difícil, as variações de superfície aprimorada (SERS) e de ponta (TERS) de Raman aumentam a sensibilidade em várias ordens de magnitude, empregando substratos metálicos em nanoescala, e estão ajudando a identificar novos biomarcadores de malignidade precoce. O diagnóstico e o monitoramento em tecidos vivos ainda estão em grande parte em fases de prova de princípio, nas quais a miniaturização dos componentes Raman pode ser adaptada a cada tecido em estudo e emprega sondas de fibra óptica personalizadas com lasers e CCDs integrados ou externos. Esses e outros procedimentos emergentes baseados em RS estão ajudando a otimizar a triagem, biópsia, avaliação da margem do tumor e monitoramento contínuo do tratamento e seu sucesso ou deficiências.